Vous avez dit Triphasé ?
Hé, tu sait, on a fait une expérience marrante.
Ha oui ?
Oui ! On a disposé un pain de glace en hauteur, puis on a placé un fil de fer lesté par deux masses en travers du pain de glace, les deux masses pendant dans le vide de part et d'autre du pain de glace. Et devine ce qui se passe ? Le fil traverse la glace qui se reforme derrière le fil. C'est dingue non ?
Et bien oui, c'est dingue, surtout que l'eau est l'un des seuls fluides à réagir de la sorte.
Comment ça l'un des seuls ? C'est pas normal ?
À vrai dire, non. Mais pour répondre à cette question, il va falloir introduire le Diagramme PT comme on l'appelle entre nous, ou Diagramme de phase de son petit nom. Comme son nom l'indique il s'agit d'un diagramme de la forme P=f(T) que voici :
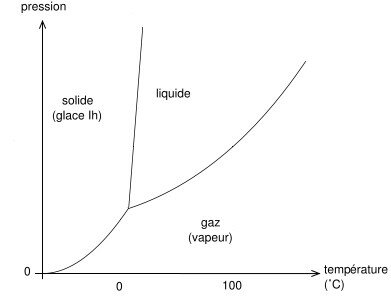
diagramme de phase d'un fluide quelconque
Ouais, c'est joli, mais ça m'avance à quoi ?
C'est sur, si tu ne me laisses pas t'expliquer. Alors, on voit trois courbes sur ce diagramme. Un première qui part du zéro pour arriver à un point d'où partent deux autres courbes : le point triple. Cette première portion de courbe correspond à la frontière entre état solide et état gazeux. Un extrait de courbe sépare le liquide du gaz, et s'arrête en un point particulier : le point critique Enfin une demie droite sépare l'état solide de l'état liquide (elle se prolonge à l'infini).
Ça n'explique rien ...
Bon, alors je te propose un truc, tu ferme ta gueule, et moi j'explique, ça te va ?
Ça va, c'est bon, pas besoin de t'énerver !
Bien, je continue. Comme je l'ai dit, il y a deux points caractéristiques. Commençons par le point triple. Comme sont nom l'indique, il se trouve entre 3 zone. En ce point cohabite le liquide, le gaz et le solide.
Ensuite vient le point critique. Passé ce point il n'y a plus aucune différence entre le solide et le liquide. Voila pour les propriétés remarquables de ce graphe.
Et ça nous amène ou ?
À considérer le problème qui nous intéresse, ton expérience. Il se trouve que l'eau a un diagramme de phase particulier. La pente de la demie droite séparant le liquide du solide est négative, contrairement à la plupart des fluide.
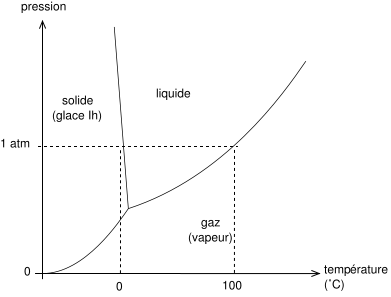
diagramme de phase de l'eau, avec les points caractéristiques de l'eau : 0°C à pression atmosphérique (solidification) et 100°C à pression atmosphérique (évaporation).
Ha oui, la pente est négative !
Maintenant, plaçons nous dans le domaine du solide, pour interpréter cette expérience. Nous somme juste en dessous de la demie droite (température en dessous de zéro, pression atmosphérique). Notre bloc de glace est stable (thermodynamiquement hein !). Maintenant on place notre fil de fer lesté de poids. On exerce alors une pression sur le bloc de glace. Donc sous le fil, la pression exercé sur la glace va augmenter, sans que la température ne change. Étant situé juste sous la courbe, quand la pression augmente, on traverse ladite courbe. Et on se retrouve dans le domaine liquide. Donc la glace sous le fil va fondre. Le fil traverse donc la glace.
Oui, mais la glace qui a fondue, elle devient quoi ?
Et bien, une fois que le fil est passé, la pression diminue (le fil n'étant plus là pour l'exercer). Donc la pression redescend, et on retraverse la demie droite, pour revenir dans le domaine du solide. Donc l'eau liquide se re-solidifie après le passage du fil de fer. On dit que la glace a subie deux transformations, une compression isotherme (pression augmente, température constante), suivie d'une détente isotherme (pression diminue, température constante).
Un dernier mot ?
Truite.




/https%3A%2F%2Fstorage.canalblog.com%2F95%2F14%2F274487%2F16221420_o.jpg)
/https%3A%2F%2Fstorage.canalblog.com%2F87%2F12%2F274487%2F12858041_o.jpg)
/http%3A%2F%2Fupload.wikimedia.org%2Fmath%2Fd%2Fd%2Fc%2Fddcd38012663a644fe071124d18ea6ce.png)
/https%3A%2F%2Fassets.over-blog.com%2Ft%2Fcedistic%2Fcamera.png)